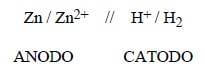L'elettrodo standard a idrogeno (abbreviato in SHE o HSE, dall'inglese Standard Hydrogen Electrode) è uno storico elettrodo a gas, così schematizzato:
Pt | H2 (1 atm) | H (1 M)
A tale elettrodo sono riferiti i potenziali standard di riduzione di tutte le coppie redox note.
È formato da un cilindro cavo di platino platinato, ossia platino ricoperto da un deposito di platino spugnoso per aumentarne la superficie specifica, immerso in una soluzione 1 M in ioni H (HCl 1 M) e sul quale viene fatto gorgogliare idrogeno gassoso alla pressione di una atmosfera.
La reazione redox che sta alla base di questo elettrodo è:
Applicando l'equazione di Nernst si ottiene:
dove:
- è il potenziale di riduzione della semireazione, misurato nel SI in ;
- è il potenziale di riduzione allo stato standard, misurato nel SI in esso assume per convenzione valore nullo ad ogni temperatura e funge quindi da riferimento, ;
- è la costante dei gas, in unità SI pari a ;
- la temperatura assoluta, misurata nel SI in ;
- la costante di Faraday, pari a ;
- è il numero di elettroni scambiati nella semireazione, pari a 2 nel caso considerato;
- è la concentrazione di quantità di sostanza dello ione idrogeno;
- è la pressione parziale dell'idrogeno gassoso.
Se si considera e la relazione precedente può essere riarrangiata, in funzione del pH (), ottenendo:
Se la soluzione contenente ioni H non è quella standard, è possibile utilizzare l'elettrodo per effettuare misure analitiche di pH.
La difficile riproducibilità ha fatto sì che l'HSE sia ormai, nella pratica di laboratorio, soppiantato da elettrodi più evoluti e con migliore sensibilità e riproducibilità.
Note
Bibliografia
- (EN) Cynthia G. Zoski, Handbook of Electrochemistry, Elsevier Science, 2007, ISBN 978-0-444-51958-0.
Voci correlate
- Elettrodo di quarta specie
- Elettrodo di riferimento
Altri progetti
- Wikimedia Commons contiene immagini o altri file su Elettrodo standard a idrogeno
Collegamenti esterni
- (EN) IUPAC Gold Book, "standard hydrogen electrode", su goldbook.iupac.org.